Actueel

EHDS en medische technologie
Om deze kansen te pakken én leveringsproblemen te helpen voorkomen, is het belangrijk om de Europese verordeningen waaraan de medische hulpmiddelen en technologie zijn gehouden, zorgvuldig te integreren in deze ‘IT’-reorganisatie.
De implementatie van de Medical Device Regulation en EUDAMED biedt waardevolle lessen voor de aanpak van de EHDS. Met het VWS Informatieplan 2024-2028 ligt er al een stevig plan klaar voor deze enorme opgave. Nefemed-leden voegen hieraan graag hun kennis en ervaring toe.
Ontwerp de informatie-deltawerken zo dat ze compatibel zijn met de Europese verordeningen voor medische producten
- Alle kennis, ervaring en visies van patiëntvertegenwoordigers, zorgprofessionals uit de 0e, 1e en 2e lijn, onderzoekers, aanbieders, betalers en de industrie, zijn vanaf het allereerste moment nodig.
- Gedurende het gehele traject zijn praktijk(voorbeelden), key process indicators, goede monitoring, transparantie, evaluatie en verantwoording essentieel.
- Beperk de implementatie tot wat in Europees verband verlangd wordt; stapel daar geen Nederlandse vereisten bovenop. Extra nationale vereisten (‘goldplating’) veroorzaken, samen met ondermeer de exorbitante groei van de kosten voor markttoelating, beschikbaarheidsproblemen van medische producten.
- Heb een scherp oog voor de effecten van de gekozen implementatieweg op de Nederlandse gereguleerde zorgmarkt. Ondermijning van het ondernemersklimaat is in niemands belang, en zeer zeker niet in die van de patiënt.
Lees hier de brief aan de Tweede Kamer voor het commissiedebat Digitale ontwikkelingen in de zorg op 10 april 2025.

Maak van patiënten geen collateral damage
De medtech-industrie is afhankelijk van wereldwijde toeleveringsketens om snelle, betrouwbare en betaalbare toegang te waarborgen. De beschikbaarheid van medische hulpmiddelen kan snel in het gedrang komen door een wedloop van importheffingen.
Europese tegenmaatregelen?
Nefemed en MedTech Europe hebben vorige week gereageerd op de verkennende survey van de Europese Commissie over een specifiek pakket van mogelijke tegenmaatregelen voor Amerikaanse importheffingen op staal en aluminium.
Wij hebben gedetailleerd inzicht gegeven op welke manier importheffingen op bepaalde grondstoffen en producten de gezondheidszorg raken en verzocht die onderdelen te verwijderen uit het voorgestelde pakket tegenmaatregelen.
| Uit de lange lijst, één voorbeeld. ‘Fluff pulp’ is een belangrijke grondstof voor onder meer absorberende continentie- en wondzorgproducten. Europese fabrikanten zijn voor meer dan 80 procent afhankelijk van import van fluff pulp uit de Verenigde Staten. Er zijn goede, betrouwbare bronnen van fluff pulp in Europa, maar elke ton daarvan is al verkocht... |
Handelsbelemmeringen zetten levens op het spel
De EU is een wereldleider in medische technologie. De VS is niet alleen een handelspartner. Het is ook een belangrijke leverancier en een grote exportmarkt voor Europese medische technologie.
Handelsbelemmeringen kunnen niet alleen de kosten verhogen en bedrijven schaden maar ook de toegang tot cruciale medische hulpmiddelen en apparatuur vertragen en levens van patiënten in gevaar brengen - aan beide kanten van de Atlantische Oceaan.
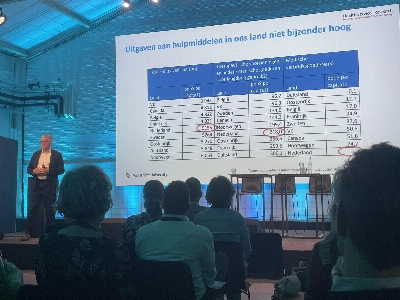
Qua uitgaven zijn we internationaal heel gemiddeld
Op de Dag van de Medische Hulpmiddelen deelde Hoogleraar Gezondheidseconomie Wim Groot feiten, cijfers en inzichten over de Kosten van hulpmiddelenzorg.
Het onderzoek waarnaar hij verwijst, 'Toegang en verstrekking extramurale medische hulpmiddelen: internationaal vergelijkend onderzoek', vond plaats juli tussen 2019 - juni 2020. Ondanks de grotere mogelijkheden, de dubbele vergrijzing, inflatie, toenemende vereisten en stijgende grondstofkosten, zijn de uitgaven aan extramurale hulpmiddelen vrij stabiel en blijven dat ook de komende jaren.
In 2023 werd zo’n 1,9 miljard euro uitgegeven aan hulpmiddelen (zie Jaarverslag VWS 2023, p. 188). Uit de Rijksbegroting 2025 blijkt dat er tot en met 2029 jaarlijks zo’n 2 miljard euro voor extramurale medische hulpmiddelen beschikbaar is (Rijksbegroting 2025). Een klein en slinkend deel van de totale zorguitgaven. ⬇️

Ontschotten en goed kijken naar toegevoegde waarde maakt investeren in medische hulpmiddelen tot een mogelijkheid tot besparen, doordat er dan op andere plekken in de samenleving lagere kosten zijn.
Functioneringsgericht voorschrijven is daar een essentieel onderdeel van, zo bleek ook uit een peiling onder de aanwezigen. Daarbij zijn natuurlijk in de allereerste plaats de patiënt en zijn directe omgeving gebaat - maar het heeft dus een positief effect voor onze hele maatschappij. Alle reden om met een nieuw inkoopbeleid daarop aan te sturen.

Reflectiesessie Beschikbaarheid cruciale voorraden en voorzieningen 31 maart 2025
Voorzieningen voor de beschikbaarheid van kritieke geneesmiddelen zijn een 'hot issue'. De beschikbaarheid van essentiële medische hulpmiddelen en technologie kwam tot nu toe nog maar matig in beeld.
Maar in de Kamerbrief van 14 maart 2025 over ’Marktwerking in de zorg’ schrijft de minister (pagina 3, punt 7) dat ze samenwerkt met marktpartijen aan een nieuwe kijk op de “just in time” economie, ‘met meer aandacht voor de beschikbaarheid van cruciale voorraden en voorzieningen, zodat de zorg weerbaar wordt voor omstandigheden zoals de dreiging van een nieuwe pandemie of van een oorlogssituatie, of mogelijke nationale crises zoals een ramp of terreuraanslag’.
Wat betekent dat voor de leden van NEFEMED? In een reflectiesessie verkennen we het onderwerp Beschikbaarheid cruciale voorraden en voorzieningen, een aspect van de supply chain dat een steeds dringerder onderwerp van gesprek wordt.
Deze digitale reflectiesessie vindt plaats op maandag 31 maart 2025 van 13:00 tot 14:00 u. Leden kunnen zich aanmelden via secretariaat@nefemed.org.
Documenten
- Verslag van een schriftelijk overleg over o.a. Voortgangsbrief beschikbaarheid geneesmiddelen, maart 2025
- Brief Agema over Marktwerking in de zorg, maart 2025
- EC stelt Critical Medicines Act voor, maart 2025
- Brief Agema over Beschikbaarheid medische hulpmiddelen, december 2024
- LCG Lijst kritieke geneesmiddelen, november 2024
- Nefemed: Beleid voor kritieke medische hulpmiddelen, november 2024

Hoopvolle inbreng voor Gerichte evaluatie MDR/IVDR
Focus op EUDAMED voor transparantie en samenwerking
De minister benadrukt het belang van EUDAMED en de aanzienlijke rol die deze database zal spelen om de transparantie van medische hulpmiddelen te vergroten en de samenwerking tussen lidstaten efficiënter te maken. Lees daarover meer in dit nieuwsbericht.
Betrouwbare en geloofwaardige regelgeving
Elk voorstel dat voortvloeit uit de evaluatie moet duidelijk bijdragen aan de betrouwbaarheid en geloofwaardigheid van het regelgevingssysteem. Toekomstige voorstellen moeten serieus rekening houden met degenen die hebben geïnvesteerd in naleving en mogen geen onduidelijkheid of mogelijkheden tot ontduiking bieden voor degenen die niet willen voldoen, aldus de minister. Betrouwbare, geloofwaardige regelgeving is de basis voor een goed investerings- en vestigingsklimaat en daarmee essentieel voor de beschikbaarheid van innovatieve medische hulpmiddelen en technologie. Dat de minister dit deelt, blijkt ook uit het volgende punt.
Betere balans tussen veiligheid, beschikbaarheid en innovatie in de wetgeving
In haar inbreng stelt de minister dat hogere eisen niet het enige is dat bijdraagt aan patiëntveiligheid. Patiënten zijn niet veilig als medisch hulpmiddelen niet beschikbaar zijn in de Europese Unie. Daarom moet er gezocht worden naar een balans tussen veiligheid, beschikbaarheid en innovatie van medische hulpmiddelen in de wetgeving.
Zorgen over impact van horizontale wetgeving; duidelijker beeld en harmonisatie
De minister is bezorgd over de impact van horizontale wetgeving op de beschikbaarheid van medische hulpmiddelen op de EU-markt. Zij steunt voorstellen voor adequate regulering van onderwerpen als duurzaamheid, (chemische) stoffen, data, digitale markten, cybersecurity en dergelijke, maar ziet de noodzaak om ervoor te zorgen dat horizontale wetgeving zoveel mogelijk wordt geharmoniseerd met de MDR en IVDR. Zij pleit een beter coördinatiemechanisme en een duidelijk overzicht van horizontale wetgeving die een wisselwerking heeft met de MDR en IVDR. Nefemed dringt al langer aan op een gedegen interdepartementale afstemming zodat de veiligheid en beschikbaarheid van medische hulpmiddelen niet in de knel komt door goedbedoelde, averechts-uitwerkende wetgeving, in Nederland en in de EU.
Nefemed is benieuwd naar de verdere uitwerking van de laatste punten uit de inbreng van de minister en de punten die andere lidstaten hebben ingebracht:
Meer ondersteuning voor efficiëntere certificering
De minister is van mening dat de wetgevende instellingen, zoals de Europese Commissie en Medical Device Coordination Group (MDCG), hulpmiddelen moeten blijven ontwikkelen die een efficiëntere certificering mogelijk maken. Wij Beter begrip hoe certificering wordt opgepakt door private ondernemers. De certificaten zijn veel duurder en bewerkelijker geworden benieuwd welke maatregelen.
Nieuwe Stuurgroep onder CAMD
De minister is voorstander van de oprichting van een politieke stuurgroep onder de CAMD-structuur (Competent Authorities for Medical Devices), met experts op het gebied van medische hulpmiddelen die input kunnen geven over prioriteiten en de ontwikkeling van het systeem op de lange termijn en die internationale activiteiten kunnen coördineren. Deze activiteiten vinden nu deels plaats in drie verschillende groepen, waardoor volgens de minister de governance verwarring oproept.
Webinar Evaluatie en wijzigingen MDR/IVDR
Morgen, 20 maart 2025, organiseert Nefemed een Webinar Evaluatie en wijzigingen MDR/IVDR met Erik Vollebregt van Axon Lawyers. U kunt nog aansluiten!

Eindelijk contracteren volgens Kwaliteitsstandaarden
Het handelen volgens de Kwaliteitsstandaarden is verre vanzelfsprekend. Vier jaar na de ontwikkeling van het Generiek Kwaliteitskader Hulpmiddelenzorg kopen zorgverzekeraars nog steeds niet in volgens de gezamenlijk opgestelde modules (Compressie, Continentie, Diabetes, Prothese, Stoma), terwijl die zijn ingeschreven in Zorginzicht, het Kwaliteitsregister van het Zorginstituut Nederland. Door de huidige organisatie van zorg kan bovendien elk hulpmiddelenvoorschrift van zorgprofessionals bij aflevering worden doorkruist.
Stand van de wetenschap en praktijk
In haar Reactie op het verzoek van het lid Paulusma, gedaan tijdens de Regeling van Werkzaamheden van 11 februari 2025, over het bericht ‘Minister Agema en zorgorganisaties praten weer over aanvullend zorgakkoord’ (11 maart 2025), schrijft minister Agema onder meer:
‘De huidige betaaltitels mogen alleen gedeclareerd worden als de zorg die geleverd is voldoet aan de stand van de wetenschap en praktijk. Zorg die voldoet aan de stand van de wetenschap en praktijk wordt vastgelegd in de professionele standaarden en kwaliteitsstandaarden. Het is aan de zorgprofessional om daarnaar te handelen. En het is aan de zorgverzekeraar om dit te controleren.’
Tweede Kamer dringt aan op actie
Begin 2015 kreeg de Tweede Kamer signalen dat zorgverzekeraars bij de beslissing over hulpmiddelen te weinig rekening hielden met de problemen van de patiënt. Te weinig maatwerk en teveel eenheidsworst bij het verstrekken van hulpmiddelen. De Kamer drong aan op actie. In april 2022 stuurde de NZa een duidelijke Brief aan zorgverzekeraars over hulpmiddelen, over passende zorg, zorgplicht en transparantie.
Tien jaar en vele initiatieven later krijgen patiënten nog steeds niet de hulpmiddelenzorg volgens de stand van de wetenschap en praktijk, niet de best passende, functioneringsgerichte hulpmiddelenzorg én niet de hulpmiddelenzorg die hun zorgverlener heeft voorgeschreven.
Morgen vindt het Commissiedebat Medisch Zorglandschap plaats. Nefemed dringt aan op (afdwingbare) actie om het inkoop- en contracteringsbeleid nu eindelijk in overeenstemming te brengen met de geregistreerde kwaliteitsstandaarden.

Webinar Towards Healthcare Packaging Circularity 24 maart 2025
De nieuwe Verordening (EU) 2025/40 betreffende verpakkingen en verpakkingsafval (PPWR) is sinds januari 2025 van kracht. De Verordening stelt strengere eisen aan alle verpakkingen die op de EU-markt worden gebracht en bevat bepalingen over ontwerp voor recycling (DfR) en de introductie van gerecycled materiaal.
In de Verordening (EU) 2025/40 zijn wel belangrijke uitzonderingen voor hulpmiddelen opgenomen:
“Om overeenkomstig het Unierecht een hoog niveau van bescherming van de gezondheid van mens en dier te waarborgen en om risico’s voor de voorzieningszekerheid of de veiligheid van geneesmiddelen en medische hulpmiddelen te voorkomen, moeten bepaalde soorten kunststof verpakkingen worden vrijgesteld van de verplichting inzake een minimumgehalte aan gerecycled materiaal. Die soorten kunststof verpakkingen zijn primaire verpakkingen, zoals gedefinieerd in Richtlijn 2001/83/EG en Verordening (EU) 2019/6, contactgevoelige kunststof verpakkingen voor medische hulpmiddelen die onder Verordening (EU) 2017/745 vallen, contactgevoelige verpakkingen voor medische hulpmiddelen voor in-vitrodiagnostiek die onder Verordening (EU) 2017/746 vallen, contactgevoelige kunststof verpakkingen van voor zuigelingen en peuters bedoelde levensmiddelen en contactgevoelige kunststof verpakkingen van voeding voor medisch gebruik die onder Verordening (EU) nr. 609/2013 vallen. Die vrijstelling moet ook gelden voor de buitenverpakking voor geneesmiddelen voor menselijk en diergeneeskundig gebruik, zoals gedefinieerd in Verordening (EU) 2019/6 en Richtlijn 2001/83/EG, in gevallen waarin de verpakking moet voldoen aan specifieke eisen om de kwaliteit van het geneesmiddel te behouden.”
Towards Healthcare Packaging Circularity
Maar daarmee is zeker niet alles gezegd! Daarom gaat Tatiana Diaz op 24 maart 2025 tijdens een interactief webinar in op de belangrijkste wettelijke vereisten van de PPWR en de gevolgen voor de hulpmiddelensector op het gebied van DfR, bijmengverplichting, etikettering en hergebruikvereisten.
Gastspreker Tatiana Dias
Tatiana Dias joined DuPont in 2023 as EMEA Regulatory & Standards Consultant for Healthcare Packaging, focusing on Circular Economy. She holds a PhD in Sustainable Chemistry from the University of Nottingham, in the UK. She started her career at MedTech Europe in Regulatory Affairs, initially in Medical Devices, with a gradual shift towards Sustainability and Environment. In 2022, she expanded her scope of action to manage the Sterile Barrier Association’s Committees.
Tatiana is a member of and actively involved in several international and European standardization organisations and groups, such as CEN TC261, ISO TC 198 WG7 and TC102 WG4 on packaging and sterilization, as well as key industry associations active in advancing packaging circularity.
Meld u aan
Nefemed-leden kunnen zich voor dit webinar aanmelden via secretariaat@nefemed.org.

Webinar Leveringszekerheid en EU-meldplicht 27 maart 2025
Tijdens dit webinar duiken we met experts diep in de implementatie van deze verplichting (artikel 10a) binnen de MDR en IVDR, geïntroduceerd door Verordening (EU) 2024/1860. Ontdek de verplichtingen voor fabrikanten, leveranciers en andere economische operators, de impact op de toeleveringsketen en hoe u zich optimaal voorbereidt.
Programma
- Introductie
- De meldplicht: waar komt het vandaan en hoe is dit vanaf 2025 in Nederland geregeld?
Door Claire Hostmann, Senior beleidsadviseur Leveringszekerheid medische hulpmiddelen en Coördinator Duurzame medische producten bij Ministerie van VWS - De meldplicht: en wat betekent dit in de praktijk?
Door Marie-Hélène Schutjens, Juridisch adviseur gezondheidsrecht, geneesmiddelen en medische technologie, Partner bij Schutjens * De Bruin - Praktijkvoorbeeld vanuit perspectief van een fabrikant. Wat dit nu betekent voor de bedrijfsvoering, en welke ontwikkelingen nog te verwachten zijn en hoe kunt u daarop anticiperen.
Door Rick Paauw, Quality and Regulatory Manager bij Medtronic
Meld u aan via de volgende link. Deelname is gratis.

Webinar Evaluatie en wijzigingen MDR/IVDR 20 maart 2025
Op 20 maart 2025 geeft hij een update van de evaluatie en wijzigingen MDR/IVDR.
Wilt u er ook weer bij zijn? U kunt zich voor dit webinar aanmelden via secretariaat@nefemed.org.

Samen werken aan de European Health Data Space
De Verordening European Health Data Space regelt onder meer:
- Het primair gebruik van gegevens: zodat mensen controle krijgen over hun gezondheidsgegevens en de uitwisseling van deze gegevens voor gezondheidszorg in de hele EU vergemakkelijkt wordt.
Hoofdstuk II beschrijft de aanvullende rechten voor patiënt en stelt de technische infrastructuur vast die nodig is voor de implementatie ervan. Lidstaten moeten ervoor zorgen dat de vereiste infrastructuur op hun niveau aanwezig is en dat zorgverleners ermee verbonden zijn. - De gemeenschappelijke markt voor systemen voor elektronische patiëntendossiers.
Hoofdstuk III over elektronische patiëntendossiersystemen (EPD) is gericht op fabrikanten en andere economische diensten die EPD-systemen op de markt aanbieden. Het stelt eisen aan dergelijke systemen met betrekking tot interoperabiliteit en logmogelijkheden. Het stelt ook mechanismen op voor markttoezicht op EPD-systemen, met bepalingen over de markttoezichtautoriteiten die door de lidstaten moeten worden aangewezen en de activiteiten van deze autoriteiten. - Het secundair gebruik van gegevens: een consistent, betrouwbaar en efficiënt systeem voor hergebruik van gezondheidsgegevens voor onderzoek, innovatie, beleidsvorming en regelgeving.
Hoofdstuk IV is gericht op houders en gebruikers van gezondheidsgegevens. Het stelt verplichtingen voor houders van gezondheidsgegevens om gegevens beschikbaar te stellen en geeft aan hoe gebruikers van gezondheidsgegevens dergelijke gegevens kunnen gebruiken. Verder stelt het Health Data Access Bodies (HDAB's) en de benodigde infrastructuur vast.
Zorgvuldige implementatie
Een coalitie van 39 Europese gezondheids(branche)organisaties, waaronder MedTech Europe, heeft de Europese Commissie opgeroepen om nu snel een inclusief, goed gefinancierd Stakeholder Forum op te richten voor een effectieve implementatie van de European Health Data Space (EHDS). Zij adviseren:
- Nodig alle kennis, ervaring en visies aan tafel, waaronder patiëntvertegenwoordigers, zorgprofessionals, onderzoekers, aanbieders, betalers en de industrie.
- Werk met praktijkvoorbeelden en KPI’s en zorg voor een goede monitoring, evaluatie en verantwoording.
- Wees transparant: publiceer de belangrijkste bevindingen en aanbevelingen online en houd regelmatig openbare raadplegingen over belangrijke zaken en beslissingen.
Het is belangrijk om ook in Nederland de samenwerking en implementatie goed te organiseren. In 2019 is voor de implementatie van de Verordening Medische Hulpmiddelen (MDR), samen met ministerie van VWS, de Referentiegroep MDR/IVDR opgericht. Daarin zijn alle partijen die te maken hebben met medische hulpmiddelen via de koepels vertegenwoordigd en wordt constructief samengewerkt. Een dergelijke vorm zou voor de omvangrijke EHDS-Verordening goed denkbaar zijn.
Meer informatie
- Europese ruimte voor gezondheidsgegevens, Europese Commissie
- Regulation (EU) 2025/327 on the European Health Data Space and amending Directive 2011/24/EU and Regulation (EU) 2024/2847, Europese Commissie 5 maart 2025
- Frequently Asked Questions on the European Health Data Space, Europese Commissie 5 maart 2025
- Joint statement calling for an enhanced collaboration in European Health Data Space implementation, MedTech Europe 5 maart 2025
